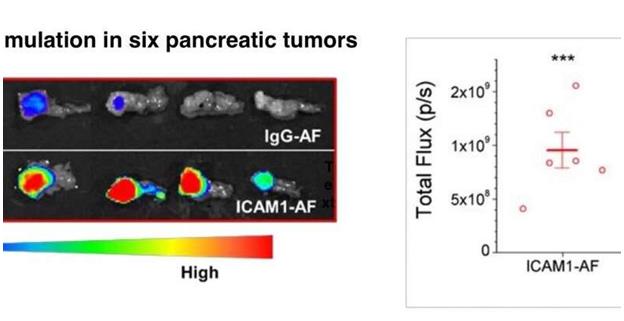
左图红色表示在具有相邻正常胰腺组织的人胰腺肿瘤中高水平的ICAM1抗体蓄积。
蓝色染色显示非靶向IgG抗体在肿瘤中的蓄积量低。在右侧,定量抗体积聚。
图片来源:黄晶,波士顿儿童医院博士
胰腺癌具有极高的致死性:根据美国国家癌症研究所的数据,仅约10%的患者在诊断后五年仍存活。现在,由Marsha Moses博士实验室进行了临床前研究。波士顿儿童医院的研究人员报道,使用高度选择性,有效,工程化的抗体-药物组合,可在小鼠模型中显着持久地消退肿瘤。
研究人员说,这项发现于11月3日发表在《先进科学》杂志上,为进一步的临床前研究奠定了基础,以将该方法推广到临床。
胰腺癌已被证明很难用药物治疗。肿瘤不仅血液供应有限,难以输送药物,而且还被基质(致密的结缔组织)包围,肿瘤细胞受到细胞外基质(蛋白质和碳水化合物的网状结构)的保护。
波士顿儿童医院血管生物学计划的负责人摩西说:“将药物引入这些肿瘤可能很困难。” “我们开发了一种新型的化学免疫治疗剂,它比其他治疗剂更好地选择性识别并穿透胰腺肿瘤。”
Moses实验室由黄精博士领导,开发了一种抗体-药物偶联物或ADC,该抗体由两部分组成:一种选择性地归巢于胰腺癌细胞表面分子(称为ICAM1)的抗体,以及一种对癌细胞有毒的药物。其表面带有ICAM1的细胞会被药物杀死,而正常细胞则无法幸免。
Moses Lab的共同通讯作者,Moses Lab的Peng Peng博士说:“ ADC的大小类似于单个抗体的大小:不到10纳米。” “由于这种超小直径,它可以比其他新疗法(例如T细胞免疫疗法或纳米药物)更好地穿透基质并到达胰腺肿瘤细胞。”
合理选择抗体和药物
在筛选了数十种不同蛋白质的肿瘤表面后,研究小组选择了ICAM1作为ADC抗体的靶标。2014年,摩西实验室在三阴性乳腺癌中显示出较高的ICAM1水平,在黑色素瘤和甲状腺癌中也很丰富。
该团队进行了类似的无偏筛选,以选择要包括在ADC中的最佳药物。从临床上已经使用的药物中提取。他们在两个人类胰腺癌细胞系以及正常胰腺细胞中测试了四个候选ADC。将ICAM1抗体与细胞毒性药物DM1(Mertansine)相结合的ADC在HER2阳性乳腺癌中临床使用,是杀死肿瘤细胞最有效的方法,比其他ADC药物效果更好。DM1-ICAM1抗体组合不会损害不产生ICAM-1的非癌性胰腺细胞。
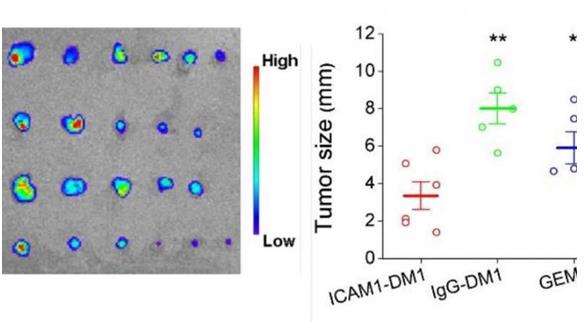
左图,荧光成像显示了六种不同的胰腺肿瘤,分别用PBS(假治疗),吉西他滨,与非靶向抗体(IgG)偶联的DM1和与靶向ICAM1抗体偶联的DM1处理。肿瘤直径在右侧量化。图片来源:黄晶,波士顿儿童医院博士
胰腺肿瘤缩小
接下来,研究小组将具有胰腺肿瘤的小鼠随机分组,以接受全身注射的四种治疗方法之一:DM1-ICAM1抗体偶联物,与非靶向抗体(IgG)结合的DM1,吉西他滨(一种用于胰腺癌的一线化疗药物)癌症)或假治疗。
与其他组相比,接受DM1-ICAM1抗体偶联物的小鼠的肿瘤大小显着降低,即使在仅仅两剂之后,其在14周的研究中仍持续存在。该治疗还有效抑制了转移至包括肺,肝和脾在内的正常器官。通过称重动物并对其器官进行病理分析评估,没有观察到毒性。
无创肿瘤监测
最后,Huang开发了一种基于MRI的分子肿瘤成像技术,以补充ICAM1 ADC治疗,从而确认了肿瘤上存在ICAM1,而无需进行侵入性活检。这可能有助于预测治疗效果并监测随时间的变化。最终,摩西希望能够使用该小组先前报告的两种非侵入性尿液生物标志物来监测治疗效果。
摩西说,虽然其他ADC已在胰腺癌中进行了测试,但没有一个在临床上显示出足够的疗效,而且还导致脱靶毒性。她说:“我们方法的精确性既来自于特定的目标,又具有通过MRI监控目标的能力。”
ICAM1-DM1 ADC是摩西实验室正在开发的有针对性的专利癌症 药物输送系统产品组合的一部分;其他包括纳米脂质,脂质体和外泌体。