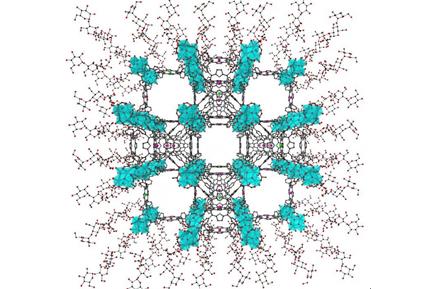
多功能,抗癌候选药物的化学结构。图片来源:阿肯色大学哈桑·贝扎维(Hassan Beyzavi)。
阿肯色大学的研究人员已经开发出一种新型的纳米药物候选物,可以杀死三阴性乳腺癌细胞。
三阴性乳腺癌是最激进和致命的乳腺癌之一。这项研究将帮助临床医生直接靶向乳腺癌细胞,同时避免化学疗法的不利,毒性副作用。
他们的研究发表在六月的高级治疗学杂志上。
化学和生物化学系助理教授Hassan Beyzavi领导的研究人员将一类称为金属有机骨架的新型纳米材料与一种已经开发的光动力疗法药物的配体联系在一起,从而创造出了一种靶向纳米粒子的纳米多孔材料。杀死肿瘤细胞而对正常细胞没有毒性。
金属有机框架是一类新兴的用于靶向药物递送的纳米材料。配体是与其他分子结合的分子。
贝伊扎维说:“除了皮肤癌,乳腺癌是美国女性最常见的癌症形式。” “我们知道,每年有成千上万的妇女死于乳腺癌。三阴性细胞的患者尤其容易受到伤害,因为唯一批准的这类癌症的治疗方法会产生毒副作用。我们已经通过开发一种抗癌药物解决了这个问题。以癌细胞为目标的共制剂,对健康细胞没有影响。”
Beyzavi实验室的研究人员致力于开发新型的靶向光动力疗法药物。有针对性的光动力疗法(PDT)是一种非侵入性方法,可替代化学疗法(且副作用明显减少),它是一种无创方法,它依赖于光敏剂,该光敏剂在被光照射后会产生所谓的有毒活性氧,从而杀死癌细胞。近年来,PDT因其无需手术,化学疗法或放射线即可治疗肿瘤的能力而备受关注。
Beyzavi的实验室专门研究将纳米材料(例如金属有机骨架)与PDT以及其他疗法结合起来。金属有机框架显着增强了PDT的有效性。
来自Beyzavi实验室的博士生Yoshie Sakamaki制备了纳米材料,然后将其与PDT药物的配体进行生物缀合,形成了纳米孔材料,该材料专门靶向并杀死了肿瘤细胞,而对正常细胞没有毒性。
除癌症治疗外,这种新颖的药物输送系统还可与磁共振成像(MRI)或荧光成像一起使用,从而可以追踪体内药物并监测癌症治疗的进展。
这个合作项目还包括美国大学研究小组通过分析化学教授朱莉·斯滕肯(Julie Stenken)所做的贡献。杜玉春,生物科学副教授;以及生物与农业工程学教授金振宇(Jin-Woo Kim)。
美国癌症协会估计,2019年有268,600例新发浸润性乳腺癌病例和41,760例死亡。目前,美国有超过310万乳腺癌幸存者。自2007年以来,年龄在50岁以下的女性的乳腺癌死亡率一直稳定,但在老年女性中则继续下降。据信这种减少是早期发现和更好治疗的结果。
三阴性乳腺癌是具有侵略性的,缺乏雌激素受体,孕激素受体和人表皮生长因子受体2,这意味着它无法通过受体靶向疗法进行治疗。现有的化学疗法很难治疗,并且经常需要手术,因为它会迅速转移到全身。
细胞毒性化学疗法是唯一批准用于此类乳腺癌的治疗方法。妇女三阴性乳腺癌的80%以上的癌症与化疗方案,其包括蒽环类抗生素,如多柔比星,这可能会导致心脏毒性是一个严重的副作用治疗。此外,使用5-FU,顺铂,紫杉醇,阿霉素或依托泊苷对乳腺癌细胞系进行化学疗法治疗已显示出多药耐药性。