对于肿瘤已经发生扩散并不可切除的局部晚期或转移性膀胱癌患者而言,化疗是主要的治疗手段,不过免疫疗法的出现为患者提供了更多的治疗选择。根据罗氏公司公布的一项关于PD-L1肿瘤免疫疗法Atezolizumab(Tecentriq)治疗膀胱癌的III期IMvigor130临床研究的数据结果表明,与化疗相比,Atezolizumab联合化疗治疗显著延长了患者的无进展生存期(PFS)。
IMvigor130是一项多中心、部分盲法、随机的临床研究,针对于在先前未接受系统疗法治疗转移性疾病的局部晚期或转移性膀胱癌患者。研究主要评估了Atezolizumab联合含铂类化疗、Atezolizumab单药治疗和安慰剂联合含铂类化疗用于一线治疗的疗效和安全性。该研究共入组了1213例患者,按照1:1:1的比例随机分成三组:(A组)Atezolizumab联合含铂类化疗(吉西他滨联合顺铂或卡铂);(B组)Atezolizumab单药治疗;(C组)安慰剂联合含铂类化疗(吉西他滨联合顺铂或卡铂)。Atezolizumab联合组主要终点是疾病无进展生存期(PFS)和总生存期(OS)。次要终点是客观缓解率(ORR)和缓解持续时间(DOR)。
结果显示,与含铂化疗相比,Atezolizumab联合化疗使无进展生存期(PFS)显示出具统计学意义的显著改善(中位无进展生存期:8.2个月vs 6.3个月)。在意向性治疗(ITT)患者群体中,与化疗相比,Atezolizumab联合化疗在总生存期方面也获得了令人欣喜的结果,但在中期分析时这些数据没有达到统计学意义(中位总生存期:16.0个月vs 13.4个月)。该研究中,Atezolizumab联合化疗治疗组的安全性与单个药物已知的安全性相一致,没有发现新的安全信号。
罗氏公司还公布了意向性治疗(ITT)患者群体和PD-L1表达水平不同的患者群体中Atezolizumab单药疗法的额外数据。结果显示,在PD-L1高表达(IC2/3)群体中,Atezolizumab单药治疗观察到了较好的总生存期(OS)结果,但这些数据没有按照试验的分层设计进行正式检验。后续工作将持续至下一次分析。
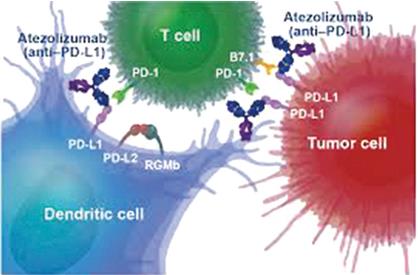
Atezolizumab是首个获批用于治疗晚期膀胱癌的免疫疗法。它是一种直接靶向PD-L1的人源单克隆抗体,可以通过阻断PD-L1与T细胞上的PD-1和CD80的相互作用,抵抗肿瘤的免疫逃避手段,并诱导免疫应答,帮助人体的免疫系统攻击癌细胞。