美国食品和药物管理局已授予Nektar Therapeutics(Nasdaq:NKTR)的研究药物bempegaldesleukin(NKTR-214)的突破疗法称号(BTD),与百时美施贵宝(NYSE:BMY)的Opdivo(nivolumab)结合使用先前未经治疗的不可切除或转移性黑色素瘤患者的治疗。
这一称号的授予,是基于2019年美国临床肿瘤学会(ASCO)年会上公布的正在进行的I/II期临床研究PIVOT-02的转移性(IV期)黑色素瘤患者研究数据。结果显示,截止2019年3月29日,中位随访12.7个月,接受NKTR-214联合Opdivo免疫组合治疗的38例疗效可评估患者中,总缓解率(ORR)为53%(20/38)、完全缓解率(CR)为34%(13/38)、疾病控制率(DCR:CR+PR+SD,完全缓解+部分缓解+疾病稳定)为74%。在这一亚组中,有53%的患者表现出对治疗的反应,包括肿瘤环境被认为是最不利的参与者——没有PD-L1和T细胞水平较低。
PIVOT-02还在评估用NKTR-214,Opdivo和Yervoy的联合使用情况,包括黑色素瘤以外的癌症类型的治疗。这些癌种有:肾细胞癌,非小细胞肺癌,膀胱癌和三阴性乳腺癌。
该疗法是如何作用的?
bempegaldesleukin(NKTR-214)通过促进免疫T细胞和自然杀伤NK细胞的活跃度和增殖而发挥作用。
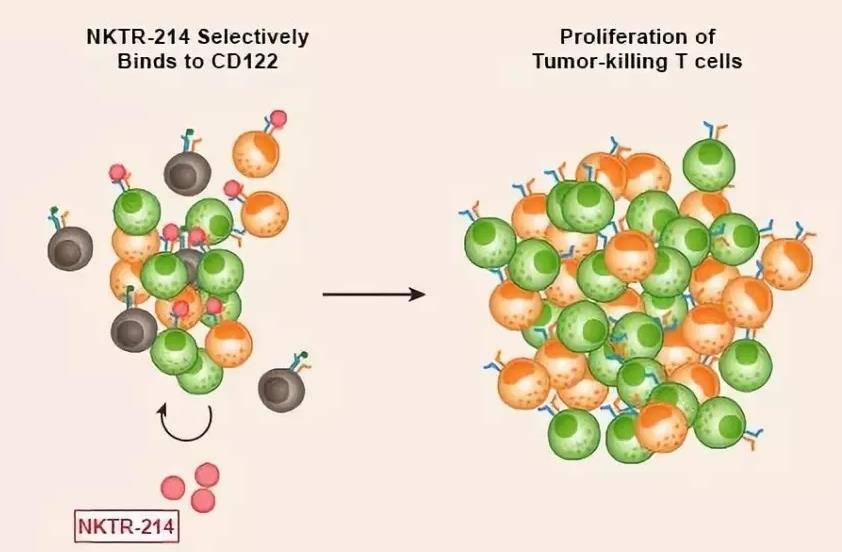
具体而言,NKTR-214与CD122结合,CD122是免疫T细胞和NK细胞上IL-2受体的亚基,可增强这些细胞的水平及其抗肿瘤反应。研究药物还增加了T细胞上PD-1蛋白和癌细胞上PD-L1的水平,这表明它可能会增强免疫检查点抑制剂(如Opdivo)的有效性。
该疗法会出现哪些不良反应?
关于安全性,在6名(14.6%)患者中报告了所有3/4级治疗相关不良事件(TRAEs),其中包括房颤(4.9%);高血糖症(2.4%);急性肾损伤,血肌酐增加,呼吸困难,高钠血症和缺氧(n = 1)。1/2级不良事件包括流感样症状(80.5%),皮疹(70.7%),疲劳(65.9%),瘙痒(48.8%),恶心(41.5%),关节痛(36.6%)和肌痛(31.7%) )。共有9.8%的患者因不良事反应药。