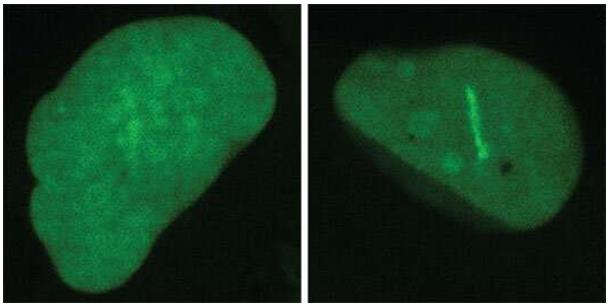
强烈染色(右)显示DNA修复机制不足的细胞
LMU小组已鉴定出一种对DNA修复至关重要的酶。当癌细胞累积DNA损伤时,该因子的丢失会导致细胞死亡。对靶蛋白的化学抑制为特定癌症的治疗提供了可能的策略。
在德国,与大多数西方国家一样,癌症是最常见的死亡原因,其发病率仅次于心血管疾病。尽管“癌症”一词涵盖了在其病程和发生频率上有很大不同的多种疾病,但是所有癌症综合征都有一个共同的特征:与正常细胞不同,癌细胞以不受控制的方式增殖。
失去调节细胞生长的能力分裂和分裂通常与遗传物质DNA的有害突变有关,而遗传物质决定了体内所有细胞类型的分子组成,进而决定了其功能。可以引起这种突变的因素包括紫外线,X射线和伽马射线,以及特定的化学物质,毒素和称为氧自由基的高反应性形式的氧。另外,遗传性(“先天性”)突变也可以促进癌症的发展。由于诱变剂无处不在,并且在DNA复制过程中经常发生突变,因此细胞已进化出多种修复受损DNA的机制。根据病变的大小和性质,细胞激活对DNA损伤的多种反应。修复酶能够纠正细胞DNA中的小范围缺陷,
介导DNA修复的机制对于生存至关重要。但是,由于肿瘤细胞的分裂速度快于许多其他细胞类型,因此经常使用积极促进DNA损伤的药物作为治疗药物。这种方法有选择地消除已经遭受了很大程度的DNA损伤的癌细胞。在这种特定情况下,功能性DNA修复系统是障碍而不是帮助。这解释了为什么研究人员长期以来一直试图找出修复途径网络中的薄弱环节,这些薄弱环节可以作为治疗癌症的药物靶标,而且这种搜索一直没有白费。
煽动癌细胞自杀
一种这样的靶标是一类被称为聚(ADP-核糖)聚合酶(简称PARP)的酶,在人类中已经鉴定出其中的18种。LMU生物医学中心生理化学主席安德烈亚斯·拉杜纳(Andreas Ladurner)教授说:“ PARP1和PARP2是DNA修复酶,其作用方式已被该领域研究了50年。” 他补充说:“特别是自2005年以来,对PARPs进行了深入研究,将其作为癌症背景下的潜在药物靶标。”
PARP抑制剂在乳腺癌和卵巢癌的治疗中特别有用。在许多情况下,这些癌症缺乏功能性BRCA1或BRCA2基因。这些基因编码的蛋白质参与DNA单链断裂的修复。这些基因的丢失使该特定途径失去作用,并迫使肿瘤细胞使用另一种机制,其中PARP酶是关键。这种对PARPs的依赖性使它们极易受到抑制这些酶的药物的攻击。
尽管PARP抑制剂在临床上是有效的,但它们并非没有副作用-部分是因为它们干扰了DNA修复以外的PARP酶的功能。因此,它们并不适合所有患者使用。
癌症治疗的新目标
Ladurner和他的同事希望改变这一点,并已开始寻找替代攻击点。在他们的最新研究中,他们着手回答两个问题:除了PARPs之外,还需要哪些其他因素来修复DNA损伤,哪些因素可能为治疗药物提供有希望的靶标?
Ladurner解释说:“ PARP1和PARP2就像喇叭一样。一旦结合受损的DNA,它们就会发出强烈的DNA损伤信号,从而促进修复反应;它们不直接参与DNA修复的执行。” “这是另一种称为ALC1的酶发挥作用的地方,因为它特别响应PARP发出的信号。” 为了确定ALC1的确切功能,他和他的团队使用遗传方法创建了缺乏功能性ALC1蛋白的细胞。仔细观察这些细胞的性质发现,在没有ALC1的情况下,PARP酶仍然与DNA损伤位点结合。
Ladurner说:“有趣的是,这种'诱捕'效果与PARPs 1和2抑制剂产生的效果相当。” 但是,尽管当前使用的PARP抑制剂会阻止PARP产生的信号的产生,但ALC1的失活会禁用DNA修复机制本身。因此,这种新颖的方法提供了一种更直接的抑制修复途径的手段,并导致肿瘤细胞死亡而又不破坏其他PARP的功能。确实,ALC1功能的丧失增强了PARP 1和2抑制剂的作用。
Ladurner希望将这样的实验室发现转化为新疗法。他是位于慕尼黑附近Planegg的初创企业Eisbach Bio的共同创始人。他和他的同事们已经确定了抑制肿瘤中ALC1等靶标的候选药物,他们希望在不久的将来在人体中进行测试。