目前靶向及免疫治疗确实是如火如荼,很多患者了解靶向及免疫治疗高效低毒的特性,问“邱医生,我可不可以不化疗,直接靶向或免疫治疗”?以前邱医生的回答是根据目前的指南不建议,因为靶向治疗及免疫治疗的发展年限比较短,所以数据不够充分。但是,随着靶向及免疫数据的不断更新,新的治疗标准已经出现。
今天邱医生给大家展示靶向及免疫治疗优于化疗的强有力的数据。相信对化疗排斥的患者有一定的帮助。
靶向治疗
对于有驱动基因突变的非小细胞肺癌患者,首选靶向治疗。
肺癌靶向药物大盘点
EGFR(19DEL,L858R):针对这两种突变的肺癌患者,推荐一代EGFR抑制剂易瑞沙、特罗凯、凯美纳和二代EGFR抑制剂阿法替尼、达可替尼和三代靶向药奥西替尼。
ALK阳性首选治疗方案为一代ALK抑制剂克唑替尼,耐药后可以考虑二代ALK抑制剂艾乐替尼、色瑞替尼、布加替尼。ALK的第三代抑制剂劳拉替尼除了对一代和二代ALK抑制剂耐药后患者有效,同时对脑转移的患者有效。
ROS1融合 治疗药物有克唑替尼、色瑞替尼,卡博替尼,劳拉替尼,Entrectinib以及TPX005,以及DS-6051b。
BRAF突变 1%-3% 的非小细胞肺癌会出现 BRAF 基因突变,采用达拉菲尼(150mg bid)联合曲美替尼(2mg qd)的治疗方案。
MET基因突变 常用药物为克唑替尼及卡博替尼。
HER-2基因突变 HER-2突变占1%-2%。常用药物为 T-DM1、阿法替尼、曲妥珠单抗、吡咯替尼(Pyrotinib)和波奇替尼。
NTRK融合 近两年,除了PD-1,最火的就是一款万众期待的“治愈系”广谱抗癌药Larotrectinib,也就是大名鼎鼎的LOXO-101,约有3% NSCLC患者肿瘤中可以发现NTRK1基因融合现象。
免疫治疗
免疫治疗nivolumab (O药)用于非小细胞肺癌的二线治疗
CheckMate 017和CheckMate 057是非小细胞肺癌(NSCLC)大样本患者(n = 854)中的长期疗效与安全性的评估,这两个研究用五年的时间去评估免疫治疗对比化疗的一个分析。
CheckMate 017和CheckMate 057分别为nivolumab(O药)对照多西他赛治疗晚期二线鳞癌和非鳞癌的III期临床研究,NSCLC患者随机分为nivolumab(3mg/kg,每2周)或多西他赛(75mg/m2,每3周),直至病情进展或不可耐受毒性而停药。主要的研究终点是总生存期(OS),次要研究终点是客观缓解率(ORR),无进展生存时间(PFS)、安全性等。
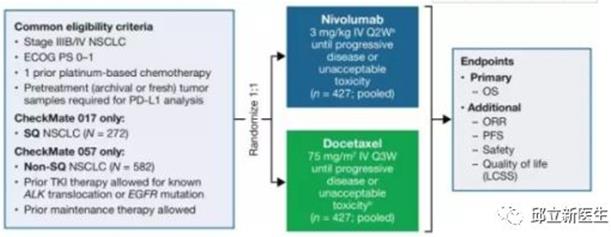
结果,CheckMate 017和CheckMate 057的患者数据共进行了最少5年的随访。鳞癌和非鳞癌亚组的汇总分析表明,nivolumab存在持续的OS获益,5年总生存时间(OS)为13.4%,多西他赛组为2.6%。(nivolumab组的5年生存率是多西他赛组的5倍)。

结论,对nivolumab(O药)存在客观应答的患者中有32.2%在五年时仍持续应答,而对多西他赛应答的患者在五年时持续应答的比例则为0%。接受nivolumab(O药)治疗的患者保持应答的中位时间为 19.9个月,而多西他赛组仅为5.6个月。
FDA在2105年已经批准批准nivolumab(O药)用于非小细胞肺癌(NSCLC)二线治疗。
免疫治疗Pembrolizumab (K药)用于非小细胞肺癌的一线治疗
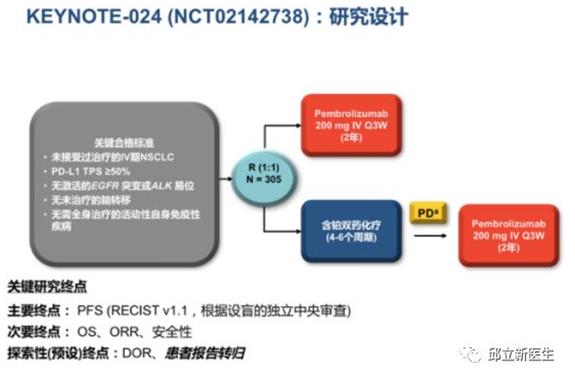
KEYNOTE-024研究入组了305例既往未经治疗的非小细胞肺癌患者,入选标准:1)PD-L1 TPS≥50%,2)无EGFR或ALK突变,3)无脑转移的患者。
一组为154例NSCLC患者使用帕博利珠单抗组(200mg q3w)使用两年,
另一组为151例NSCLC患者含铂两药方案化疗4-6个周期,肿瘤进展后使用帕博利珠单抗(200mg q3w),合起来共使用两年。
结果:三年的随访结果显示,帕博利珠单抗组的总生存时间(OS)为26.3个月,化疗组的总生存时间(OS)为14.2个月。3年的OS率,帕博利珠单抗组为43.7%,化疗组为24.9%。
安全性方面,免疫治疗组较化疗组的安全性更优,3~5级治疗相关的不良事件(TRAEs)发生率,免疫治疗组和化疗组分别为31%和53%。
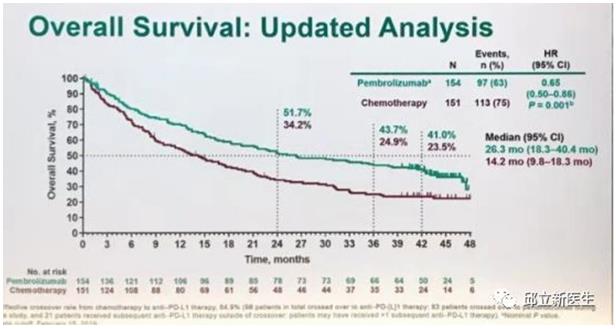
总结 在PD-L1 TPS≥50%的转移性NSCLC患者的一线治疗上,免疫治疗优于化疗。
KEYNOTE-042研究入组了1274例既往未经治疗的非小细胞肺癌患者,入选标准:1)PD-L1 TPS≥1%,2)无EGFR或ALK突变,3)无脑转移的患者。
一组为637例NSCLC患者使用帕博利珠单抗组(200mg q3w)最多治疗35个周期,
另一组为637例NSCLC患者卡铂联合紫杉醇或培美曲塞两药方案化疗最多 化疗6个周期。(分配接受培美曲塞化疗的非鳞NSCLC患者可以选择接受培美曲塞单药维持治疗)。
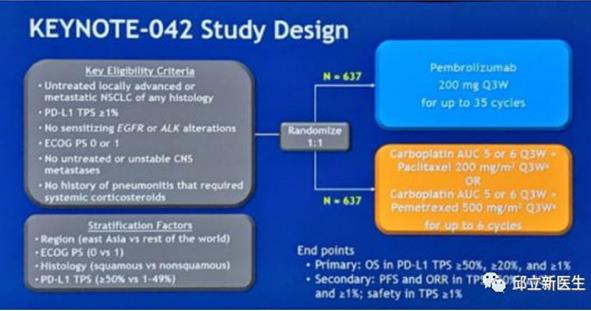
结果用药2年患者的统计分析显示:在 PD-L1 TPS≥50%的患者中,帕博利珠单抗组和化疗组的生存期具有显著差异,总生存时间(OS)分别为20.0个月和12.2个月; PD-L1 TPS≥20%的患者,两组OS仍具有显著差异,总生存时间(OS)分别为17.7个月和13.0个月;此外,在PD-L1 TPS≥1%的患者,两组差异仍具有统计学意义,总生存时间(OS)分别为16.7 个月和12.1个月。
PFS分析显示,在PD-L1 TPS≥50%的患者中,帕博利珠单抗组和化疗组的无进展生存时间(PFS)分别为7.1个月和6.4个月;在TPS≥20%的患者中,两组的无进展生存时间(PFS)分别为6.2个月和6.6个月;在TPS≥1%的患者中,两组的无进展生存时间(PFS)分别为5.4个月和6.5个月。
安全性分析,帕博利珠单抗组和化疗组任意级别的治疗相关不良事件(AE)发生率分别为63%和90%。3级或以上的AE发生率分别为18%和41%;最常见的AE对比,帕博利珠单抗组为甲状腺功能减低(11%),化疗组为贫血(37%)。
总结: 1. 免疫治疗对比化疗在PD-L1 TPS≥1%的患者中具有更好的疗效和更低的毒副反应;2. 这项研究,首次纳入了中国人群,使得研究的结果能够更适用于中国患者;3. 分析不同亚组的结果发现,随着PD-L1表达的增加,单药帕博利珠单抗的疗效也越来越好。
确定了K药单药在PD-L1阳性患者的价值——TPS ≥50%,单药明显优于化疗;PD-L1 TPS在1%~49%的,可以和化疗平起平坐,这也是改变临床实践的研究。
PD1(信迪利单抗)联合安罗替尼一线治疗NSCLC,客观缓解率(ORR)高达72.7%
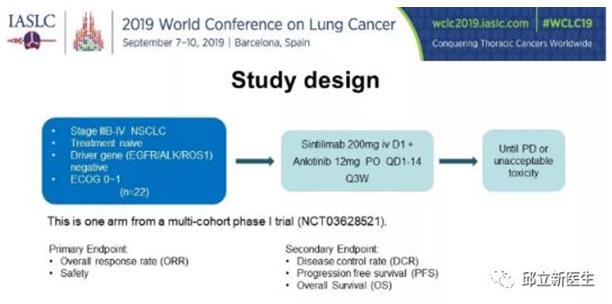
研究设计入组要求 1)IIIB-IV期的非小细胞肺癌(NSCLC),2)未经治疗过的患者,3)驱动基因(EGFR/ALK/ROS1)阴性,4)ECOG 0~1分的18~75岁患者。给予信迪利单抗(200mg d1)和安罗替尼(12mg/d,口服,d1-14)三周为一个疗程,直至疾病进展(PD)或不可耐受的毒性。研究主要终点为客观缓解率(ORR)和安全性,次要终点包括(疾病控制率)DCR、无进展生存期(PFS)和总生存期(OS)。
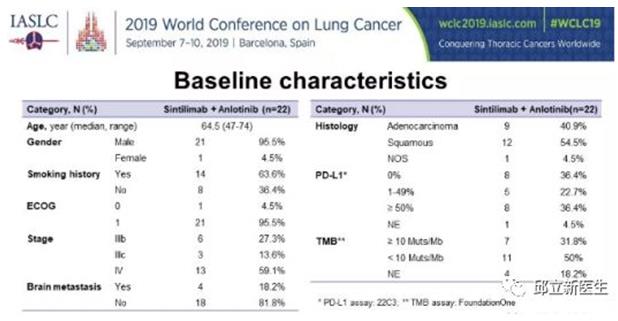
入组人员特点,共入组了22名患者,其中包括一些相对难治疗的患者,比如脑转移的患者,PD-L1无表达及低表达的患者、TMB低表达的患者。(这些患者是医生最头痛的患者,因为治疗有效率太低了!)
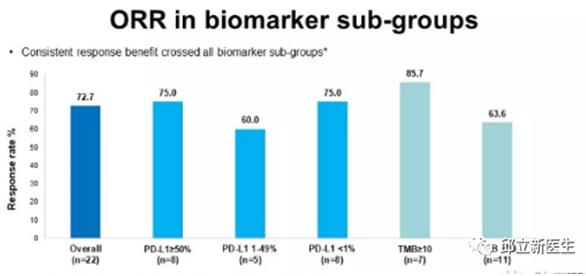
邱医生不得不提的是下面这幅图,太有实际意义了。因为我们临床工作中,很多患者的PD-L1表达都是阴性,很多患者及医生认为PD-1对这部分患者效果不好,但是实际情况是,PD-L1表达阴性的患者和PD-L1大于50%的患者疗效是一样的,都能达到75%的客观缓解率。(PD-L1阴性的患者,免疫治疗还是可以尝试的!),同样TMB低表达的患者也是有效的。
结论 数据截止2019年7月3日,16例患者确认为部分缓解(PR),6例患者疾病稳定(SD),ORR高达72.7%(49.8%~89.3%),DCR为100% (84.6%~100%)。
PD-1(卡瑞利珠单抗)联合化疗一线治疗NSCLC,疾病控制率(DCR)为87.3%
上海市肺科医院的周彩存教授牵头的一项卡瑞利珠单抗联合培美曲塞和卡铂一线治疗中国晚期/转移性非鳞NSCLC患者有效性和安全性的中期分析结果。
研究设计 入组要求1)一项开放标签、随机、多中心III期研究,2)EGFR或ALK突变阴性的晚期/转移性非鳞NSCLC患者,3)既往未接受过任何治疗,4)ECOG 评分 0-1分,5)≥1个可以测量的靶病灶,6)没有脑转移的患者。

分为两组,一组为卡瑞丽珠单抗+培美曲塞+卡铂,一组为培美曲塞+卡铂。均接受4~6个周期的治疗,然后一组予以卡瑞丽珠单抗+培美曲塞维持治疗,另一组予以培美曲塞维持治疗。直至疾病进展或出现不可耐受的毒性。
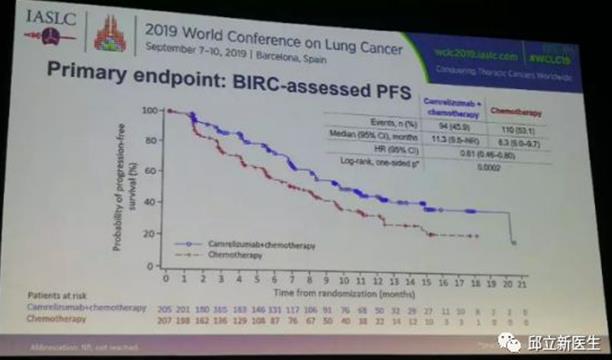
结果显示,与单纯化疗相比,卡瑞利珠单抗联合化疗能显著延长患者的中位PFS[11.3个月VS 8.3个月, HR=0.61,P=0.0002]。而且,卡瑞利珠单抗联合化疗组患者的ORR(60.0% vs 39.1%)、DCR(87.3% vs 74.4%)、DoR(17.6个月 vs 9.9个月)和OS(未达到 vs 20.9个月)均显著优于单纯化疗组患者。
O+Y双免疫治疗PD-L1表达阴性的NSCLC,疗效优于化疗
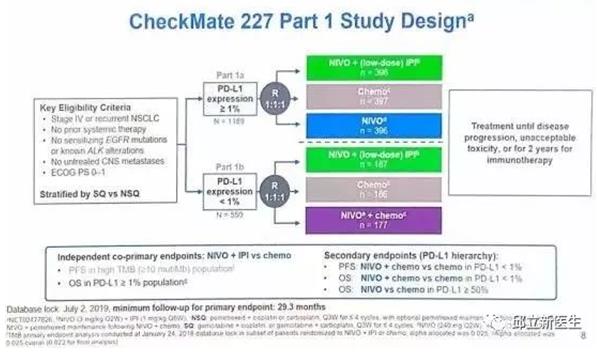
CheckMate-227三期临床试验中的第一部分评估了PD1单抗O药(纳武利尤单抗,欧狄沃)联合低剂量伊匹木单抗用于一线治疗晚期非小细胞肺癌(NSCLC)患者的疗效。
亚组分析显示,对于PD-L1 <1%的患者,欧狄沃联合低剂量伊匹木单抗能改善患者的总生存,中位OS为17.2 vs 12.2个月。该联合治疗方案的2年生存率在PD-L1≥1%与PD-L1<1%的人群中均为40%,而在化疗组相对应的2年生存率分别为33%与23%。
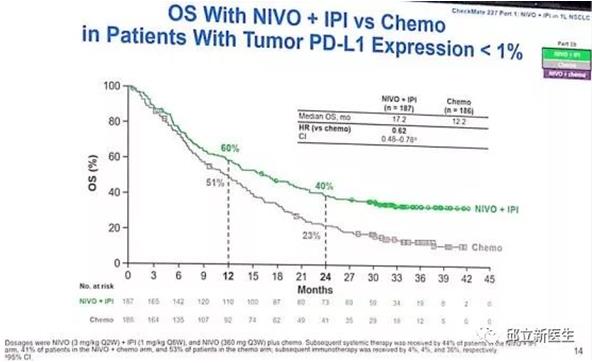
亚组分析发现,无论PD-L1表达及TMB高低,相比化疗,双免疫组合都可以带来OS获益,适用人群广泛。
转自邱立新医生微信公众号
