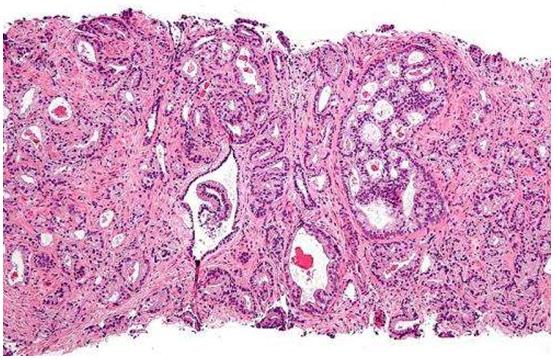
德克萨斯大学MD安德森癌症中心的研究人员报告说,前列腺癌扩散到骨骼会触发骨骼组织的破坏,进而破坏骨骼中的T细胞的发育,继而破坏免疫检查点抑制剂的有效性。
由MD Anderson生殖泌尿医学肿瘤学和免疫学教授Padmanee Sharma博士领导的研究小组解释了为什么免疫疗法在很大程度上不能成功治疗前列腺癌骨转移,并指出了可能逆转前列腺癌的可能组合。他们的发现还强调了需要以不同的眼光看待转移性癌症。
Sharma博士说:“我们倾向于认为发展到四期的疾病是统一的,但并非一律如此。我们需要对所转移的不同部位的免疫微环境进行更多的考虑,以便在我们开发治疗方法时考虑到那些微环境中可能的免疫反应。”
研究集中在抗TGF-β和抗CTLA-4的组合
研究小组发现,由肿瘤引起的骨骼破坏导致大量生成转化生长因子-β(TGF-β),该蛋白可导致辅助性T 细胞转化为Th17 CD4细胞,而不是触发TGF-β 的Th1 CD4效应细胞的抗肿瘤免疫反应。
结合抗TGF-β治疗与CTLA-4检查点抑制剂对T细胞的抑制作用可抑制小鼠模型中骨转移的生长。Sharma说:“我们正在努力开发抗CTLA-4和抗TGF-β联合治疗转移性前列腺癌的临床试验。”
大多数患有前列腺癌的男性进展为转移性,死亡率很高,而患有四期前列腺癌的男性中约70-80%会发生骨转移。Sharma及其同事的最新研究表明,抗CTLA-4(ipilimumab)和抗PD-1(nivolumab)检查点抑制剂的组合可帮助某些患有四期前列腺癌的男性,但它在抵抗骨转移方面大都失败了。
为了理解这个问题,Sharma的团队首先检查了患者治疗前后的骨髓,以获取有关治疗耐药性的线索。他们进一步研究了在转移性前列腺癌的小鼠模型中的观察结果,并测试了联合疗法。
发现Th1 CD4 T细胞的缺乏
当这种疗法起作用时,免疫检查点封锁会扩展Th1 CD4效应细胞,从而导致杀伤CD8 T细胞的活化和长期记忆细胞的产生。
研究小组在依匹木单抗治疗的患者的软组织中发现了大量Th1效应子,但这些关键细胞在骨骼中基本不存在,而是在其中发现了大量Th17细胞。
夏尔马指出:“重要的是这里没有Th1细胞。” 细胞因子将辅助细胞极化为不同类型,在骨骼微环境中它们会产生大量Th17细胞,但Th17细胞的功能尚不清楚。
该团队开发了两种转移性疾病小鼠模型,一种代表骨转移,另一种代表原发性前列腺癌或软组织转移的皮下模型。
与在人类中使用一样,使用ipilimumab和nivolumab联合治疗可缩小肿瘤并延长患有软组织转移的小鼠的存活期,但对肿瘤和骨转移瘤的存活率影响很小。
治疗使肿瘤浸润的软组织和骨骼中的CD4和CD8 T细胞扩散,但未能抑制骨肿瘤的生长。T细胞的大规模细胞分析表明了原因。骨肿瘤中的CD4 T细胞仅属于Th17和调节性T细胞(Treg)谱系。Tregs抑制免疫反应,没有Th1效应细胞。
在皮下模型中,在治疗前检测到Th1效应子,然后在治疗后显着增加,而Th17和Tregs降低。
TGF-β可以保护骨骼肿瘤
骨髓中Th1细胞的缺乏导致骨骼微环境中的细胞因子谱不同。研究小组发现显着升高的TGF-β可以抑制Th1谱系并驱动Th17和Treg的发育。Th17还需要白细胞介素6的存在,正如预期的那样,该白细胞在骨髓中的含量很高。
骨转移触发了异常的骨骼重塑,并且骨骼成分被称为TGF-β的主要储存库。该团队假设骨基质重塑导致前列腺骨转移中的TGF-β水平升高。
他们的实验证实,被肿瘤激活的破骨细胞(降解骨的细胞)在侵蚀骨骼表面的同时释放出过量的TGF-β。于是他们比较了健康捐献者和有或没有骨转移的前列腺癌患者的骨髓中TGF-β的水平。健康对照组和无骨转移的患者之间的TGF-β水平没有差异,而患有骨肿瘤的患者的骨骼中TGF-β水平异常高。
阻断TGF-β可恢复Th1细胞并增强免疫疗法
用ipilimumab和nivolumab组合治疗具有骨转移的小鼠未能阻止肿瘤生长。但是在免疫疗法中加入抗TGF-β可以阻止肿瘤的生长。
单独的抗TGF-β和ipilimumab也抑制了骨转移的生长。这种组合还增加了Th1细胞的频率,并降低了骨骼微环境中的Treg 。