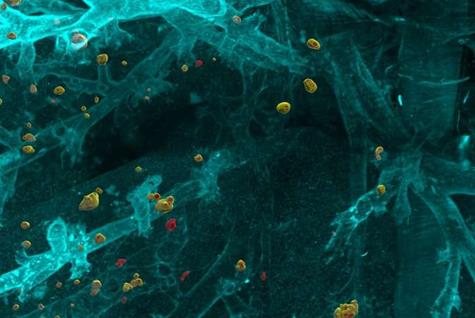
DeepMACT利用人工智能来发现小鼠体内最小的转移灶。图片显示单个扩散的细胞通过肺扩散。
癌症是全球死亡的主要原因之一,而超过90%的癌症患者最终死于远处转移,而不是原发肿瘤的直接原因。癌症转移通常是由单个扩散的癌细胞形成的,这些癌细胞逃避了人体的免疫监视系统。到目前为止,由于成像技术(例如生物发光和MRI)的分辨率有限,因此无法对体内的这些细胞进行全面检测,导致缺乏对各种癌症传播机制的了解,而恰恰这是有效治疗的先决条件,同时它还阻碍了评估新药用于肿瘤治疗的功效。
通过深度学习超越人类传统的检测能力
为了开发克服这些障碍的新技术,由Helmholtz ZentrumMünchen的组织工程和再生医学研究所所长AliErtürk博士领导的研究团队先前开发了vDISCO,这是一种可可以对单个细胞进行成像的技术,使用激光扫描显微镜,研究人员能够在清除小鼠身体组织的过程中检测到单个癌细胞的最小转移灶。
但是,手动分析此类高分辨率成像数据将是非常耗时的过程。鉴于目前用于此类数据分析的算法的可靠性和处理速度有限,这些团队开发了一种新颖的深度学习方法称为DeepMACT,已经能够检测和分析癌症转移并自动绘制vDISCO制剂中治疗性抗体的分布。DeepMACT算法与人类专家在检测转移方面的性能相匹配,但速度却快了300倍。“仅需单击几下,DeepMACT即可在不到一个小时的时间内完成几个月的手动检测工作。我们现在能够在日常日常工作中,对单个扩散的肿瘤细胞进行高通量转移分析。”
检测细胞,收集数据,了解癌症
使用DeepMACT,研究人员可以分析对不同肿瘤模型的独特转移谱。多种癌症类型的传播模式的表征可以使针对不同转移性癌症的定制靶向药物成为可能。通过分析小鼠中乳腺癌转移的进程,DeepMACT已经发现随着时间的推移,整个小鼠体内转移的实质性增加。之前传统的生物发光成像无法检测到这些特征,DeepMACT是第一种能够对全身转移过程进行定量分析的方法。这种方法还使我们能够更详细地分析肿瘤抗体疗法的靶向性。
借助DeepMACT,研究人员现在可以使用一种工具来评估采用肿瘤特异性单克隆抗体的临床疗法的靶向性。作为一个有代表性的例子,他们使用DeepMACT来量化名为6A10的治疗性抗体的功效,该抗体已被证明可减少肿瘤的生长,这强调了在单一转移水平上针对新型肿瘤药物开发的靶向疗效分析的重要性。当小分子药物与荧光染料结合时,该方法还可能追踪小分子药物的分布。
未来的道路
综上所述,这些结果表明,DeepMACT不仅为癌症转移提供了强大的方法,而且为临床前研究中的治疗药物评估提供了灵敏的工具。“对抗癌症的斗争已经进行了数十年,我们要最终战胜该疾病还有很长的路要走。为了开发出更有效的癌症疗法,我们需要了解多种癌症类型的转移机制以及开发出能够阻止转移过程的肿瘤特异性药物。”Ertürk解释说。
DeepMACT是公开可用的,可以用于在其他专注于多种肿瘤模型和治疗方案的实验室中。如今的肿瘤学临床试验的成功率约为5%,我们认为DeepMACT技术可以大大改善临床前研究中的药物开发过程,可以帮助研究人员找到功能更强大的临床试验候选药物而有助于拯救许多生命。